வாயுக்களின் இயக்கவியற் கொள்கை | இயற்பியல் - தீர்க்கப்பட்ட எடுத்துக்காட்டு கணக்குகள்: வாயு ஒன்றினால் ஏற்படும் அழுத்தத்திற்கான கோவை | 11th Physics : UNIT 9 : Kinetic Theory of Gases
11வது இயற்பியல் : அலகு 9 : வாயுக்களின் இயக்கவியற் கொள்கை
தீர்க்கப்பட்ட எடுத்துக்காட்டு கணக்குகள்: வாயு ஒன்றினால் ஏற்படும் அழுத்தத்திற்கான கோவை
எடுத்துக்காட்டு 9.1
27°C வெப்பநிலையில் உள்ள கால்பந்து ஒன்றினுள் 0.5 மோல் காற்று மூலக்கூறுகள் உள்ளன. கால்பந்தின் உள்ளே உள்ள காற்றின் அக ஆற்றலைக் கண்டுபிடி.
தீர்வு:
நல்லியல்பு வாயுவின் அக ஆற்றல் 3/2 NkT. காற்று மூலக்கூறுகளின் எண்ணிக்கை மோல்களின் எண்ணிக்கையில் கொடுக்கப்பட்டுள்ளது. எனவே சமன்பாட்டை பின்வரும் வடிவில் எழுத வேண்டும்.
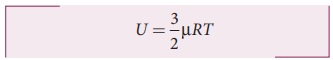
இங்கு Nk = μR (μ என்பது மோல்களின் எண்ணிக்கையாகும்)
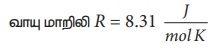
கெல்வின் வெப்பநிலை T = 273 + 27°C = 300 K
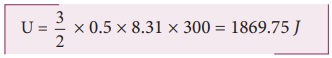
இம்மதிப்பு, 57 kg நிறையுள்ள மனிதரொருவர் 8 ms-1 வேகத்தில் ஓடும்போது அவர் பெற்றிருக்கும் இயக்க ஆற்றலுக்குச் சமமானதாகும்.
எடுத்துக்காட்டு 9.2
அறை ஒன்றினுள் 3:1 என்ற விகிதத்தில் ஆக்ஸிஜன் மற்றும் ஹைட்ரஜன் மூலக்கூறுகள் உள்ளன. அறையின் வெப்பநிலை 27°C ஆக்ஸிஜன் (O2) மற்றும் ஹைட்ரஜன் (H2) இவற்றின் மூலக்கூறு நிறைகள் முறையே 32 g mol-1 மற்றும் 2 g mol-1 ஆகும். வாயு மாறிலி R = 8.32 J mol-1 K-1 எனில் பின்வருவனவற்றைக் கணக்கிடுக.
(a) ஆக்ஸிஜன் மற்றும் ஹைட்ரஜன் மூலக்கூறுகளின் சராசரி இருமடி மூலவேகம்.
(b) ஆக்ஸிஜன் மற்றும் ஹைட்ரஜன் மூலக்கூறு ஒன்றின் சராசரி இயக்க ஆற்றல்.
(c) ஆக்ஸிஜன் மூலக்கூறுகள் மற்றும் ஹைட்ரஜன் மூலக்கூறுகளின் சராசரி இயக்க ஆற்றலின் விகிதம்.
தீர்வு :
(a) கெல்வின் வெப்பநிலை
T=27°C =27+273=300 K.
வாயு மாறிலி R = 8.32 J mol-1K-1
ஆக்ஸிஜன் மூலக்கூறின் vrms
மூலக்கூறு நிறை M = 32 g = 3 × 10-3 kg mol-1
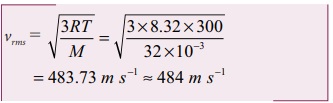
ஹைட்ரஜன் மூலக்கூறின் vrms
மூலக்கூறு நிறை M = 2 × 10-3 kg mol-1
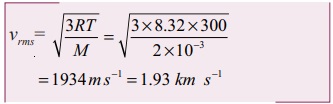
சராசரி இருமடி மூல வேகம் vrms ஆனது √M க்கு எதிர்விகிதத்தில் உள்ளதை இங்கு கவனிக்க வேண்டும். ஆக்ஸிஜனின் மூலக்கூறு நிறை ஹைட்ரஜனின் மூலக்கூறு நிறையை விட 16 மடங்கு அதிகம். இதிலிருந்து நாம் அறிவது என்னவென்றால் ஒரே வெப்பநிலையில் ஹைட்ரஜனின் சராசரி இருமடி மூல வேகம் (vrms), ஆக்ஸிஜனைவிட 4 மடங்கு அதிகமாகும். கணக்கீட்டிலிருந்து 1934/484 ≈ 4 ஆகும்.
(b) மூலக்கூறு ஒன்றின் சராசரி இயக்க ஆற்றல் 3/2 kT. இது வாயுவின் கெல்வின் வெப்பநிலையை மட்டுமே சார்ந்துள்ளது. மேலும் வாயுவின் தன்மையைச் சார்ந்ததல்ல. இரண்டு வாயுக்களின் மூலக்கூறுகளும் ஒரே கெல்வின் வெப்பநிலையில் உள்ளதால் அவற்றின் ஒவ்வொரு மூலக்கூறுகளின் சராசரி இயக்க ஆற்றலும் ஒரே மதிப்பைப் பெற்றிருக்கும். இங்கு k என்பது போல்ட்ஸ்மென் மாறிலியாகும்.
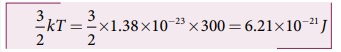
(c) அனைத்து ஆக்ஸிஜன் மூலக்கூறுகளின் சராசரி இயக்க ஆற்றல் 3/2 N0kT இங்கு N0. என்பது அறையில் உள்ள ஆக்ஸிஜன் மூலக்கூறுகளின் மொத்த எண்ணிக்கையாகும்.
அனைத்து ஹைட்ரஜன் மூலக்கூறுகளின் சராசரி இயக்க ஆற்றல் = 3/2 NHkT. இங்கு NH என்பது அறையில் உள்ள ஹைட்ரஜன் மூலக்கூறுகளின் மொத்த எண்ணிக்கையாகும்.
கொடுக்கப்பட்ட கணக்கிலிருந்து, அறையிலுள்ள ஆக்ஸிஜன் மூலக்கூறுகளின் மொத்த எண்ணிக்கை ஹைட்ரஜன் மூலக்கூறுகளின் மொத்த எண்ணிக்கையைவிட 3 மடங்கு அதிகம். எனவே ஆக்ஸிஜன் மூலக்கூறுகளின் மொத்த சராசரி இயக்க ஆற்றலுக்கும் ஹைட்ரஜன் மூலக்கூறுகளின் மொத்த சராசரி இயக்க ஆற்றலுக்கும் உள்ள விகிதம் 3:1 ஆகும்.
எடுத்துக்காட்டு 9.3
அறை ஒன்றில் இயக்கத்திலுள்ள பத்து வாயு மூலக்கூறுகளின் வேகங்கள் முறையே 2, 3, 4, 5, 5, 5, 6, 6, 7 மற்றும் 9 m s-1 ஆகும். இவற்றின் சராசரி இருமடி மூல வேகம், சராசரி வேகம் (PPP) மற்றும் மிகவும் சாத்தியமான வேகம் (vrmp) இவற்றைக் காண்க.
தீர்வு:
சராசரி வேகம்
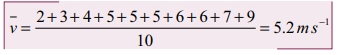
சராசரி இருமடி மூல வேகத்தைக் கணக்கிட முதலில் வேகங்களின் இருமடியின் சராசரியைக்![]() கணக்கிட வேண்டும்.
கணக்கிட வேண்டும்.
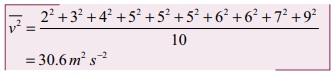
சராசரி இருமடிமூல வேகம்
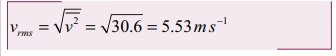
மிகவும் சாத்தியமான வேகம் vmp என்பது 5ms-1. ஏனெனில் கொடுக்கப்பட்டவற்றுள் மூன்று மூலக்கூறுகள் இவ்வேகத்தைப் பெற்றுள்ளன.
எடுத்துக்காட்டு 9.4
300 K வெப்பநிலையிலுள்ள 1 மோல் ஹைட்ரஜன் மூலக்கூறுகளின் சராசரி இருமடிமூல வேகம் (vrms) சராசரி வேகம் ![]() மற்றும் சாத்தியமான வேகம் (vmp) ஆகியவற்றைக் காண்க. இங்கு எலக்ட்ரானின் நிறையை புறக்கணிக்கவும்.
மற்றும் சாத்தியமான வேகம் (vmp) ஆகியவற்றைக் காண்க. இங்கு எலக்ட்ரானின் நிறையை புறக்கணிக்கவும்.
தீர்வு:
ஹைட்ரஜன் அணு ஒரு புரோட்டானையும் ஒரு எலக்ட்ரானையும் பெற்றுள்ளது, புரோட்டானின் நிறையுடன் ஒப்பிடும்போது எலக்ட்ரானின் நிறையை புறக்கணிக்கலாம்.
புரோட்டானின் நிறை = 1.67 × 10-27 kg.
ஒரு ஹைட்ரஜன் மூலக்கூறு = 2 ஹைட்ரஜன் அணுக்கள் = 2 × 1.67 × 10-27 kg.
சராசரி வேகம்
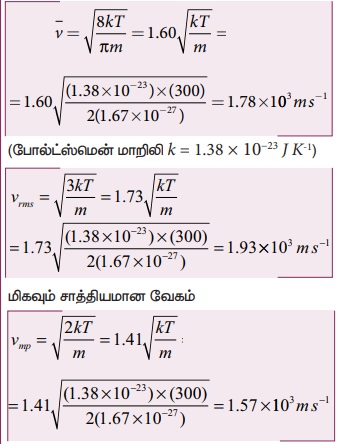
இங்கு 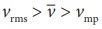 என்பதைக் கவனிக்கவும்.
என்பதைக் கவனிக்கவும்.