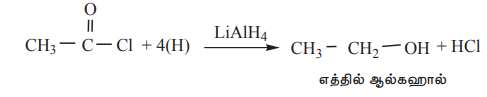அமில குளோரைடுகளை தயாரிக்கும் முறைகள், இயற் பண்புகள், வேதிப் பண்புகள் - அமில ஹேலைடுகள் | 12th Chemistry : UNIT 12 : Carbonyl Compounds and Carboxylic Acids
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 12 : கார்பனைல் சேர்மங்கள் மற்றும் கார்பாக்சிலிக் அமிலங்கள்
அமில ஹேலைடுகள்
அமில ஹேலைடுகள்:
அமில குளோரைடுகளை தயாரிக்கும் முறைகள்:
கார்பாக்சிலிக் அமிலங்களை, SOCl2, PCl5, அல்லது PCl3, போன்ற ஏதாவதொரு குளோரினேற்ற வினைக்காரணியுடன் வினைப்படுத்தி அமில குளோரைடுகள் தயாரிக்கப்படுகின்றன.
1) தயோனைல் குளோரைடுடன்(SOCl2) வினைப்படுத்துதல் மூலம்
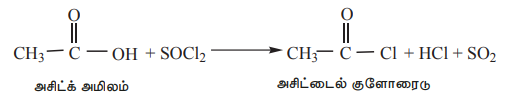
இந்த தயாரிப்பு முறையானது மற்ற எல்லா முறைகளைவிட சிறந்ததாகும், ஏனெனில் இவ்வினையில் உருவாகும் துணை விளைபொருட்கள் வாயுக்களாக இருப்பதால் எளிதில் வெளியேறுகின்றன, அதனால் அமில குளோரைடை தூய நிலையில் பெறப்படுகிறது.
இயற் பண்புகள்
• காற்றில் வெளிக்காட்டப்படும் போது இவை நீருடன் வினைபுரிவதால், ஹைட்ரஜன் குளோரைடு வெளிரிய புகையை உருவாக்குகின்றன.
• அவை நீரில் கரைவதில்லை , ஆனால் நீராற்பகுத்தலின் காரணமாக மெதுவாக கரையத் துவங்குகின்றன.
வேதிப் பண்புகள்:
அமில ஹேலைடுகள், வலிமைகுறைந்த கருகவர் காரணிகளான நீர், ஆல்கஹால்கள், அம்மோனியா மற்றும் அமீன்கள் போன்றவற்றுடன் வினைப்பட்டு அமிலம், எஸ்டர், அமைடு அல்லது பதிலீடு செய்யப்பட்ட அமைடுகளை உருவாக்குகின்றன.
1) நீராற்பகுத்தல். அசைல் ஹேலைடுகள் நீராற்பகுப்படைந்து அவற்றின் கார்பாக்சிலிக் அமிலங்களை உருவாக்குகின்றன.
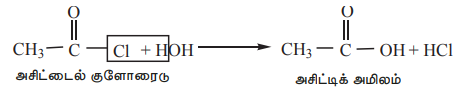
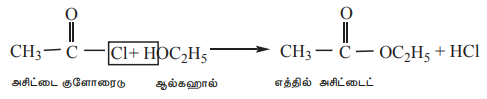
2) ஆல்கஹால்களுடன் வினைப்பட்டு (ஆல்கஹால்பகுப்பு) எஸ்டர்களைத் தருகின்றன.
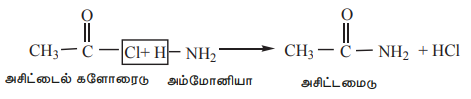
3) அம்மோனியாவுடன் வினைப்பட்டு (அம்மோனியாபகுப்பு) அமில அமைடுகளைத் தருகின்றன.
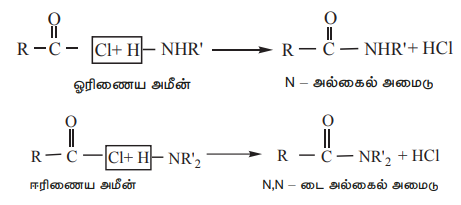
4) 1° மற்றும் 2° அமீன்களுடன் வினைப்பட்டு N-ஆல்கைல் அமைடுகளைத் தருகின்றன.
(5) ஒடுக்கம்.
(அ) இவற்றை, நச்சுப்படுத்தப்பட்ட பெல்லாடியம் வினைவேக மாற்றி முன்னிலையில் ஹைட்ரஜன் கொண்டு ஒடுக்கும்போது ஆல்டிஹைடுகளை தருகின்றன. இந்த வினையானது ரோசன்முன்ட் ஒடுக்கவினை என்றழைக்கப்படுகிறது. ஆல்டிஹைடுகளின் தயாரிப்பு முறைகள் எனும் தலைப்பின்கீழ் இந்த வினையை நாம் ஏற்கனவே கற்றறிந்தோம்.
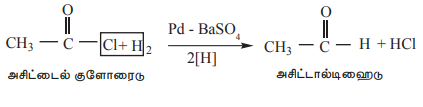
(ஆ) LiAIH கொண்டு ஒடுக்கும்போது ஓரிணைய ஆல்கஹால்களைத் தருகின்றன.