12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 12 : கார்பனைல் சேர்மங்கள் மற்றும் கார்பாக்சிலிக் அமிலங்கள்
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களின் வேதிப் பண்புகள்
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களின் வேதிப் பண்புகள்
A) கருகவர் சேர்ப்பு வினைகள்
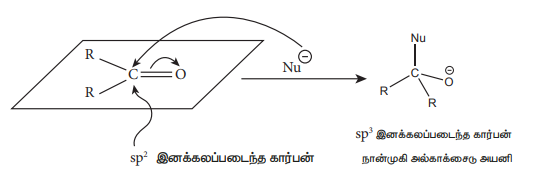
இவ்வகை வினையானது ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களின் மிகப்பொதுவான வினையாகும். கார்பனைல் கார்பன் அணுவானது சிறியளவு நேர்மின்சுமையை பெற்றுள்ளது. CNபோன்ற கருகவர் காரணிகள், இந்த கார்பனைல் கார்பன் அணுவைத் தாக்குகின்றன. இந்த கருகவர் காரணிகள் அவற்றின் தனித்த எலக்ட்ரான் இரட்டையை பயன்படுத்தி புதிய கார்பன் - கருகவர் காரணி 'σ' பிணைப்பை உருவாக்குகின்றன. அதே நேரத்தில், கார்பன் - ஆக்ஸிஜன் இரட்டை பிணைப்பிலுள்ள இரண்டு எலக்ட்ரான்கள் அதிக எலக்ட்ரான் கவர்தன்மை கொண்ட ஆக்ஸிஜன் அணுவிற்கு நகருகிறது. இதனால் ஆல்காக்சைடு அயனி உருவாக்கப்படுகிறது. இச்செயல்முறையில் கார்பன் அணுவின் இனக்கலப்பு sp2 இருந்து sp3 ஆக மாறுகிறது.
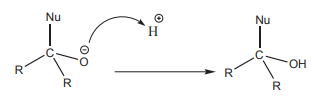
இந்த நான்முகி இடைநிலைக் கூறானது நீர் அல்லது அமிலத்தால் புரோட்டானேற்றம் பெற்று ஆல்கஹாலை உருவாக்குகிறது.
பொதுவாக, கருகவர் சேர்ப்பு வினைகளில் கீட்டோன்களை விட ஆல்டிஹைடுகள் அதிக வினைதிறன் கொண்டவைகளாக உள்ளன. ஆல்கைல் தொகுதிகளின் + விளைவு மற்றும் கொள்ளிட விளைவே இதற்கு காரணமாக விளங்குகின்றன.
எடுத்துக்காட்டுகள்
1) HCN சேர்த்தல்:
கார்பனைல் கார்பன் மீதான CN- அயனியின் தாக்குதலைத் தொடர்ந்து நிகழும் புரோட்டானேற்றத்தால் சயனோஹைட்ரின்கள் உருவாகின்றன.
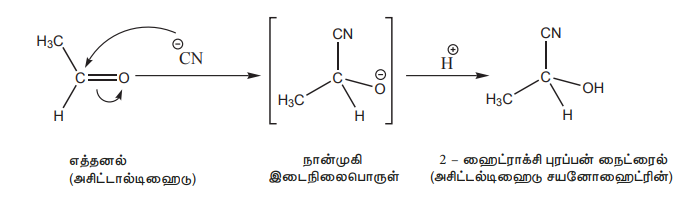
இந்த சயனோஹைட்ரின்களை அமிலங்களைக் கொண்டு நீராற்பகுத்து ஹைட்ராக்ஸி அமிலங்களாக மாற்ற முடியும். சயனோஹைட்ரின்களின் ஒடுக்கம் ஹைட்ராக்ஸி அமீன்களை தருகின்றன.
2) NaHSO3 சேர்த்தல்
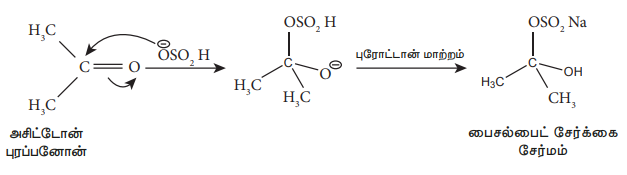
இந்த வினையானது கார்பனைல் சேர்மங்களை பிரித்தெடுக்கவும், தூய்மையாக்கவும் பயன்படுகிறது. இதில் உருவான பைசல்பேட் சேர்மமானது நீரில் கரையும் தன்மை கொண்டது. மேலும் அக்கரைசலை கனிம அமிலங்களுடன் வினைப்படுத்தும்போது கார்பனைல் சேர்மங்கள் மீள உருவாகின்றன.
3) ஆல்கஹால் சேர்த்தல்
அமில வினைவேக மாற்றி முன்னிலையில் ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களை இரண்டு சமானங்கள் ஆல்கஹாலுடன் வினைப்படுத்தும்போது அசிட்டால்கள் உருவாகின்றன.
எடுத்துக்காட்டு
HCl முன்னிலையில், அசிட்டால்டிஹைடை, இரண்டு சமானங்கள் மெத்தனால் உடன் வினைப்படுத்தும்போது 1,1, - டைமீத்தாக்ஸி ஈத்தேன் உருவாகிறது.
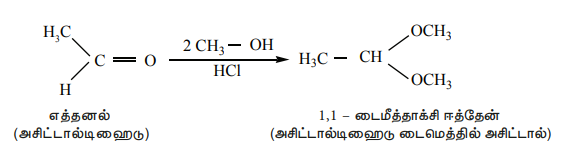
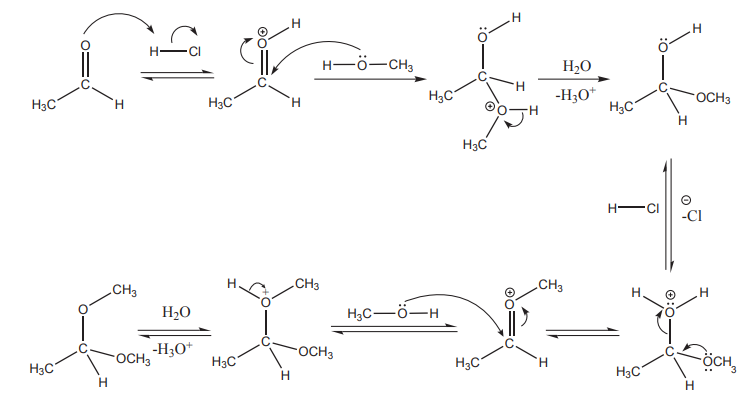
வினைவழி முறை
4) அம்மோனியா மற்றும் அதன் பெறுதிகளை சேர்த்தல்
அம்மோனியா மற்றும் அதன் பெறுதியான H2N-G ஆகியவற்றை கார்பனைல் சேர்மத்துடன் சேர்க்கும்போது கருகவர் சேர்ப்பு வினை நிகழ்கிறது. கார்பனைல் ஆக்ஸிஜன் அணுவானது புரோட்டானேற்றம் பெற்று பின்னர் நீக்க வினைக்கு உட்படுவதால் கார்பன் - நைட்ரஜன் இரட்டை பிணைப்பு உருவாகி 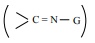
இங்கு G என்பது -ஆல்கைல், அரைல், OH, NH2, C6H5NH, NHCONH2 போன்றவை
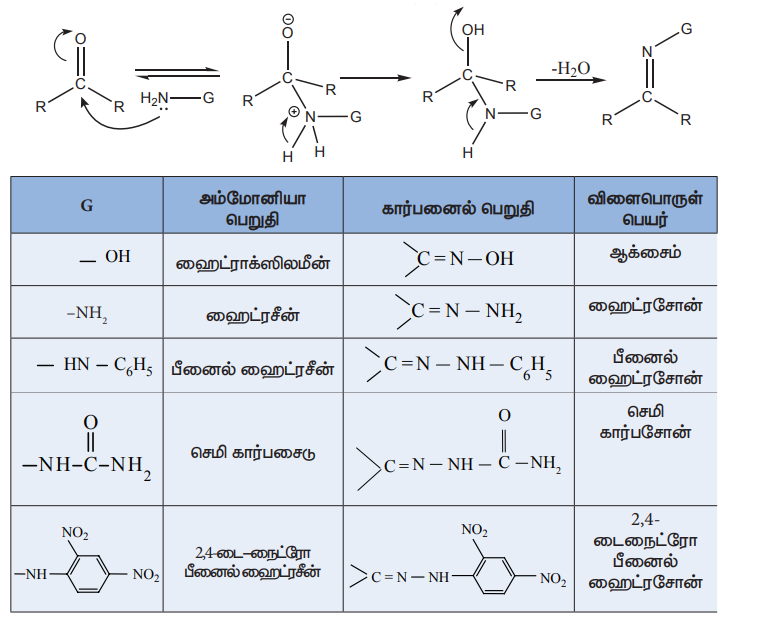
i) ஹைட்ராக்ஸிலமீன் உடன் வினை
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்கள், ஹைட்ராக்ஸிலமீனுடன் வினைபுரிந்து ஆக்சைம்களை உருவாக்குகின்றன.
எடுத்துக்காட்டு:
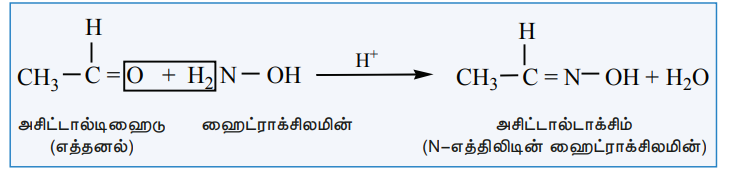
ii) ஹைட்ரசீன் உடன் வினை
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்கள், ஹைட்ரசீனுடன் வினைபுரிந்து ஹைட்ரசோன்களை உருவாக்குகின்றன.
எடுத்துக்காட்டு :
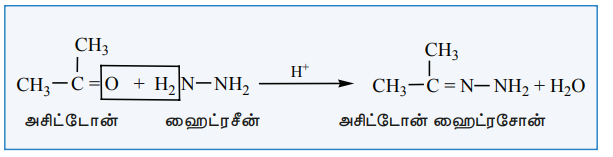
iii) பீனைல் ஹைட்ரசீன் உடன் வினை
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்கள், பீனைல் ஹைட்ரசீனுடன் வினைபுரிந்து பீனைல் ஹைட்ரசோன்களை உருவாக்குகின்றன.
எடுத்துக்காட்டு :
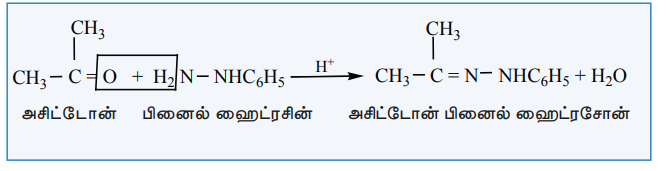
5) NH3 உடன் வினை
i) அலிஃபாடிக் ஆல்டிஹைடுகள், (ஃபார்மால்டிஹைடு தவிர), ஈதரில் கரைந்த அம்மோனியாவுடன் வினைபுரிந்து ஆல்டிமீன்களை உருவாக்குகின்றன.
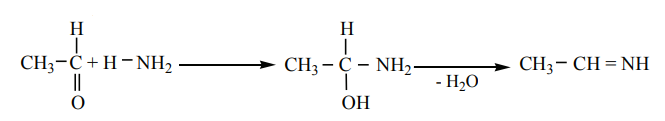
ii) ஃபார்மால்டிஹைடு, அம்மோனியா உடன் வினைபுரிந்து ஹெக்ஸா மெத்திலீன் டெட்ரா அமீனை உருவாக்குகிறது. இச்சேர்மம் யுரோட்ரோபின் எனவும் அழைக்கப்படுகிறது.
6HCHO+ 4 NH3 → (CH2)6N4 + 6 H2O
பார்மால்டிஹைடு ஹெக்சாமெத்திலீன் டெட்ரமின்
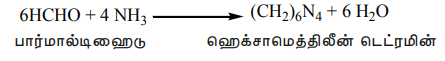
அமைப்பு
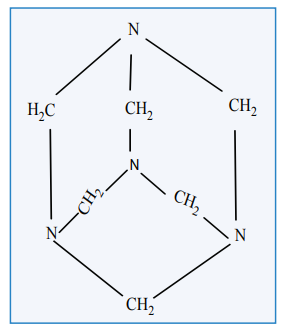
பயன்கள்
(i) யுரோட்ரோபின் ஆனது சிறுநீரக தொற்று நோய்க்கு சிகிச்சையளிக்க பயன்படுகிறது.
(ii) கட்டுப்படுத்தப்பட்ட சூழ்நிலையில் யுரோட்ரோபினை நைட்ரோ ஏற்றம் செய்யும்போது RDX (Researchand developmentexplosive)எனும் வெடிபொருள் கிடைக்கிறது. இது சைக்ளோநைட் அல்லது சைக்ளோ டிரை மெத்திலீன் டிரை நைட்ரமீன் எனவும் அறியப்படுகிறது.
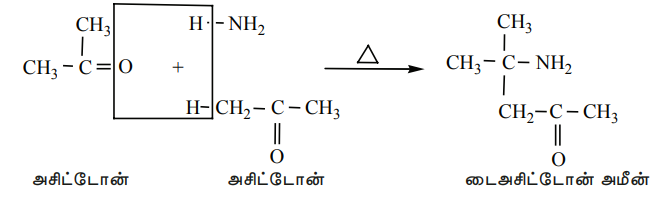
iii) அசிட்டோன், அம்மோனியா உடன் வினைபுரிந்து டைஅசிட்டோன் அமீனை தருகிறது.
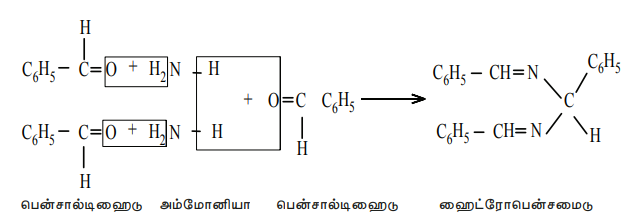
iv) பென்சால்டிஹைடு, அம்மோனியாவுடன் இணைந்து சிக்கலான குறுக்க விளைபொருளை தருகிறது.
B) ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களின் ஆக்ஸிஜனேற்றம்
a) ஆல்டிஹைடுகளின் ஆக்ஸிஜனேற்றம்
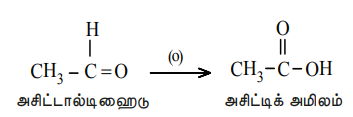
ஆல்டிஹைடுகள் எளிதில் ஆக்ஸிஜனேற்றமடைந்து மூல ஆல்டிஹைடிலுள்ள அதே எண்ணிக்கையிலான கார்பன் அணுக்களைக் கொண்ட கார்பாக்சிலிக் அமிலங்களாக மாறுகின்றன. அமிலங்கலந்த K2Cr2O2 அமிலம் அல்லது காரங்கலந்த KMnO4 அல்லது குரோமிக் ஆக்சைடு ஆகியன பொதுவாக பயன்படுத்தப்படும் ஆக்ஸிஜனேற்றிகளாகும்.
எடுத்துக்காட்டு
b) கீட்டோன்களின் ஆக்ஸிஜனேற்றம்
கீட்டோன்கள் எளிதில் ஆக்ஸிஜனேற்றமடைவதில்லை. இவை தீவிர சூழ்நிலையில் அல்லது அடர். HNO3, H+/KMnO4, H+/K2Cr2O7 போன்ற வலிமை மிக்க ஆக்ஸிஜனேற்றிகளுடன் வினைபுரியும்போது கார்பன்-கார்பன் பிணைப்பு பிளக்கப்பட்டு மூல கீட்டோன்களிலுள்ள கார்பன் அணுக்களைவிட குறைவான அணுக்களைக் கொண்ட கார்பாக்சிலிக் அமிலங்களின் கலவை உருவாகிறது.
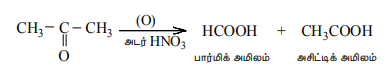
பாபஃப் (Popoff's) விதியினைக் கொண்டு சீர்மையற்ற கீட்டோன்களின் ஆக்ஸிஜனேற்றம் விளக்கப்படுகிறது. இவ்விதிப்படி, சீர்மையற்ற கீட்டோன்களை ஆக்ஸிஜனேற்றம் செய்யும் போது சிறிய ஆல்கைல் தொகுதியுடன் கீட்டோ தொகுதி இணைந்திருக்கும் வகையில் (C-CO) பிணைப்பு பிளவுறுகிறது.
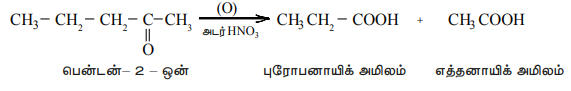
c) ஒடுக்க வினைகள்
(i) ஆல்கஹால்களாக ஒடுக்கமடைதல்
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்கள் எளிதில் ஆக்ஸிஜனேற்றமடைந்து முறையே ஓரிணைய மற்றும் ஈரிணைய ஆல்கஹால்களை உருவாக்குகின்றன என்பதை நாம் முன்னரே கற்றறிந்தோம். லித்தியம் அலுமினியம் ஹைட்ரைடு (LiAIH4), மற்றும் சோடியம் போரோ ஹைட்ரைடு (NaBH4) ஆகியன மிகப் பொதுவாக பயன்படுத்தப்படும் ஒடுக்கும் காரணிகளாகும்.
அ) ஆல்டிஹைடுகள், ஓரிணைய ஆல்கஹால்களாக ஒடுக்கப்படுகின்றன.
எடுத்துக்காட்டு
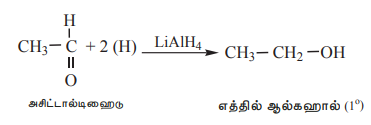
ஆ) கீட்டோன்கள், ஈரிணைய ஆல்கஹால்களாக ஒடுக்கப்படுகின்றன.
எடுத்துக்காட்டு
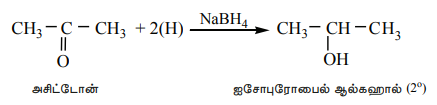
Pt, Pd, அல்லது Ni போன்ற உலோக வினைவேகமாற்றிகள் முன்னிலையில் ஹைட்ரஜனுடன் வினைப்படுத்தியும் மேற்காண் வினைகளை நிகழ்த்த முடியும். LiAlH4 மற்றும் NaBH4 ஆகியன தனித்த கார்பன் - கார்பன் இரட்டை பிணைப்புகள் மற்றும் பென்சீனில் உள்ள இரட்டை பிணைப்புகளை ஒடுக்குவதில்லை α,β நிறைவுறா ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களில், LiAlH ஆனது C = C பிணைப்பை ஒடுக்காமல் C = O தொகுதியை மட்டும் ஒடுக்குகிறது.
ii) ஹைட்ரோகார்பனாக ஒடுக்கமடைதல்
தகுந்த ஒடுக்கும் காரணிகளைப் பயன்படுத்துவதன் மூலம் ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களிலுள்ள கார்பனைல் தொகுதியை மெத்திலீன் தொகுதியாக ஒடுக்கி ஹைட்ரோகார்பன்களைப் பெற முடியும்.
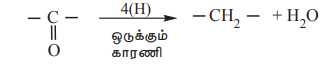
அ) கிளமென்சன் ஒடுக்கம்:
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களை ஜிங்க்பாதரசக்கலவை மற்றும் அடர்ஹைட்ரோகுளோரிக் அமிலத்துடன் சேர்த்து வெப்பப்படுத்தும்போது ஹைட்ரோகார்பன்கள் பெறப்படுகின்றன.
எடுத்துக்காட்டு
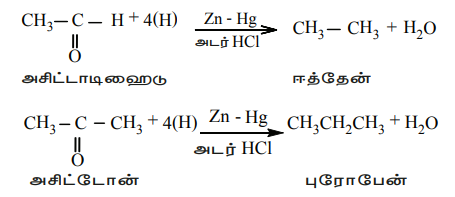
ஆ) உல்ஃப்-கிஷ்னர் ஒடுக்கம்:
ஆல்டிஹைடுகள் மற்றும் கீட்டோன்களை ஹைட்ரசீன் (NH,NH,) மற்றும் சோடியம் ஈத்தாக்சைடுடன் சேர்த்து வெப்பப்படுத்தும்போது ஹைட்ரோகார்பன்கள் பெறப்படுகின்றன. இதில் ஹைட்ரசீன் ஒடுக்கும் காரணியாகவும், சோடியம் ஈத்தாக்சைடு வினைவேக மாற்றியாகவும் பயன்படுகின்றன.
எடுத்துக்காட்டு
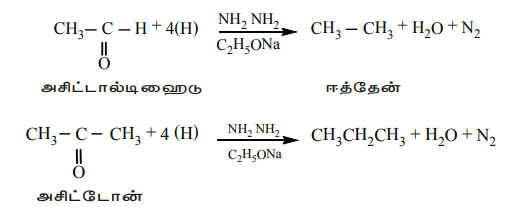
அசிட்டோன் ஆல்டிஹைடுகள் (அல்லது) கீட்டோன்கள் முதலில் அவற்றின் ஹைட்ரசோன்களாக மாற்றப்படுகின்றன. இந்த ஹைட்ரசோனை வலிமைமிகு காரத்துடன் வெப்பப்படுத்தும்போது ஹைட்ரோகார்பன்கள் உருவாகின்றன.
(iii) பினகால்களாக ஒடுக்கமடைதல்:
கீட்டோன்களை, மெக்னீஷியம் இரசக் கலவை மற்றும் நீர் கொண்டு ஒடுக்கும்போது சீர்மையுள்ள டையால்கள் உருவாகின்றன, இவை பினகால்கள் என்று அறியப்படுகின்றன.
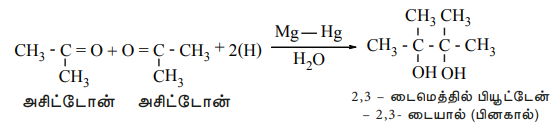
D) ஹேலோஃபார்ம் வினை
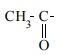 தொகுதியைக் கொண்டுள்ள அசிட்டால்டிஹைடு மற்றும் மெத்தில் கீட்டோன் சேர்மங்களை ஹேலஜன் மற்றும் காரக் கலவையுடன் சேர்த்து வினைப்படுத்தும் போது ஹேலோஃபார்ம்கள் உருவாகின்றன. இது ஹேலோஃபார்ம் வினை என அறியப்படுகிறது.
தொகுதியைக் கொண்டுள்ள அசிட்டால்டிஹைடு மற்றும் மெத்தில் கீட்டோன் சேர்மங்களை ஹேலஜன் மற்றும் காரக் கலவையுடன் சேர்த்து வினைப்படுத்தும் போது ஹேலோஃபார்ம்கள் உருவாகின்றன. இது ஹேலோஃபார்ம் வினை என அறியப்படுகிறது.
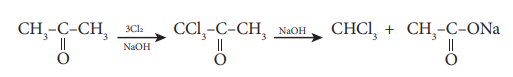
E) ஆல்கைல்தொகுதி ஈடுபடும் வினைகள்
i) ஆல்டால் குறுக்க வினை
கார்பனைல் கார்பனுடன் இணைந்துள்ள கார்பன் அணுவானது α. - கார்பன் என்றழக்கப்படுகிறது. α. - கார்பனுடன் இணைந்துள்ள ஹைட்ரஜன் அணுவானது α. - ஹைட்ரஜன் என்றழைக்கப்படுகிறது.
α.- ஹைட்ரஜனைக் கொண்டுள்ள இரண்டு ஆல்டிஹைடு அல்லது கீட்டோன் மூலக்கூறுகள், நீர்த்த NaOH அல்லது KOH முன்னிலையில் ஒன்றிணைந்து β-ஹைட்ராக்ஸி ஆல்டிஹைடு (ஆல்டால்) aல்லது β ஹைட்ராக்ஸி கீட்டோனை (கீட்டால்) தருகின்றன. இவ்வினையானது ஆல்டால் குறுக்க வினை என்றழைக்கப்படுகிறது. இந்த ஆல்டால் அல்லது கீட்டால் ஆனது எளிதில் நீர் மூலக்கூறை இழந்து ஆல்டால் குறுக்க விளைபொருட்களான α,β - நிறைவுறா சேர்மங்களை தருகின்றன.
அ) அசிட்டால்டிஹைடை நீர்த்த NaOH உடன் வெப்பபடுத்தும்போது β - ஹைட்ராக்ஸி பியுட்ரால்டிஹைடை (அசிட்டால்டால்)தருகிறது.
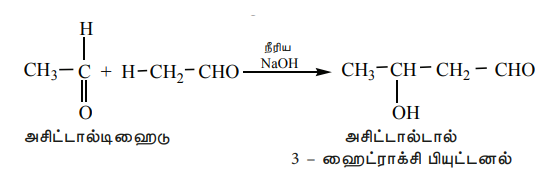
வினைவழி முறை
அசிட்டால்டிஹைடின் ஆல்டால் குறுக்க வினையானது மூன்று படிகளில் நிகழ்கிறது.
படி 1: காரத்தின் உதவியுடன் α. - ஹைட்ரஜன் அணுவானது புரோட்டானாக நீக்கப்பட்டு கார்பன் எதிரயனி உருவாகிறது.
HO+H –CH2 - CHO → CH2 - CHO + H2O
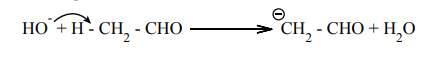
படி 2 : இந்த கார்பன் எதிரயனியானது மற்றொரு அயனியுறா ஆல்டிஹைடிலுள்ள கார்பனைல் கார்பனை தாக்கி ஆல்காக்சைடு அயனியை உருவாக்குகிறது.
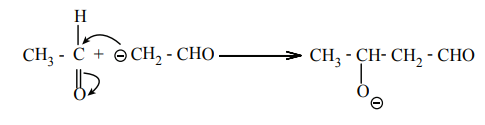
படி 3 : இவ்வாறு உருவான ஆல்காக்சைடு அயனியானது நீரினால் புரோட்டானேற்றம் பெற்று ஆல்டாலை உருவாக்குகிறது.
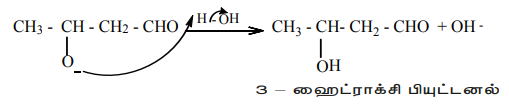
வெப்பப்படுத்தும்போது இந்த ஆல்டால் விரைவாக நீர்நீக்கம் அடைந்து α-β நிறைவுறா ஆல்டிஹைடை உருவாக்குகிறது.
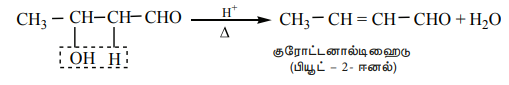
ii) குறுக்க ஆல்டால் குறுக்கம்.
இரண்டு வெவ்வேறு ஆல்டிஹைடுகள் அல்லது கீட்டோன்கள் அல்லது ஒரு ஆல்டிஹைடு மற்றும் ஒரு கீட்டோனுக்கு இடையிலும் ஆல்டால் குறுக்க வினை நிகழ முடியும். அத்தகைய ஆல்டால் குறுக்க வினையானது குறுக்க ஆல்டால் குறுக்க வினை அல்லது கலப்பு ஆல்டால் குறுக்க வினை என்றழைக்கப்படுகிறது. சாத்தியமுள்ள அனைத்து குறுக்கவினை விளைபொருட்களும் கலவையாக கிடைப்பதாலும், அவற்றை பிரித்தெடுத்தல் எளிதல்ல என்பதாலும் இந்த வினையானது அதிக பயனற்றது.
எடுத்துக்காட்டு
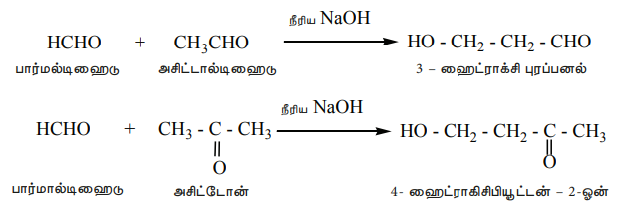
F) பென்சால்டிஹைடின் சில முக்கியமான வினைகள்:
i) கிளெய்சன்- ஸ்கிமிட் குறுக்க வினை:
அறைவெப்பநிலையில், பென்சால்டிஹைடானது, நீர்த்த காரக் கரைசல் முன்னிலையில், அலிஃபாடிக் ஆல்டிஹைடு அல்லது மெத்தில் கீட்டொனுடன் வினைபுரிந்து நிறைவுறா ஆல்டிஹைடு அல்லது கீட்டோனை உருவாக்குகிறது. இவ்வகை வினையானது கிளெய்சந் ஸ்கிமிட் குறுக்கவினை என்றழைக்கப்படுகிறது.
எடுத்துக்காட்டு:
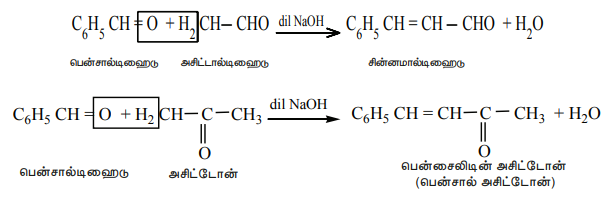
ii) கான்னிசரோ வினை:
நீர் அல்லது ஆல்கஹாலில் கரைந்த அடர் காரக் கரைசல் முன்னிலையில் α - ஹைட்ரஜனை பெற்றிறாத ஆல்டிஹைடுகள், சுய ஆக்ஸிஜனேற்றம் மற்றும் ஒடுக்கத்திற்கு உட்பட்டு ஆல்கஹால் மற்றும் கார்பாக்சிலிக் அமில உப்பு ஆகியவை சேர்ந்த கலவையை தருகின்றன. இந்த வினையானது கான்னிசரோ வினை என்றழைக்கப்படுகிறது.
பென்சால்டிஹைடை அடர் NaOH (50%) உடன் வினைப்படுத்தும்போது பென்சைல் ஆல்கஹாலையும் சோடியம் பென்சோயேட்டையும் தருகிறது.
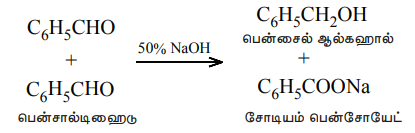
இந்த வினையானது விகிதக்கூறு சிதைவு வினைக்கு எடுத்துக்காட்டாகும்.
கான்னிசரோ வினையின் வினைவழி முறை
கான்னிசரோ வினையானது மூன்று படிகளில் நிகழ்கிறது.
படி 1: கார்பனைல் கார்பனின் OH - மீதான தாக்குதல்.
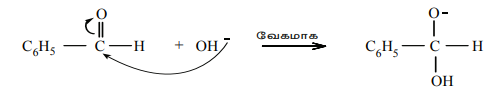
படி 2: ஹைட்ரைடு அயனி இடமாற்றம்
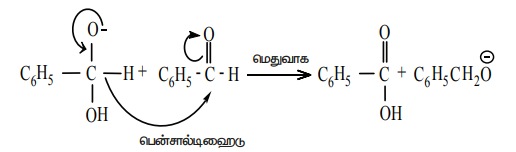
படி 3 : அமில - கார வினை .
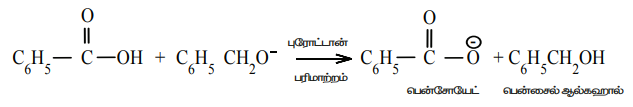
கான்னிசரோ வினையானது α - ஹைட்ரஜனை கொண்டிராத ஆல்டிஹைடுகளுக்கான சிறப்பு வினையாகும்.
குறுக்க கான்னிசரோ வினை
இரண்டு வெவ்வேறு ஆல்டிஹைடுகளுக்கிடையே (இரண்டும் o ஹைட்ரஜனை கொண்டிராதவை) கான்னிசரோ வினை நிகழும்போது அவ்வினையானது குறுக்க கான்னிசரோ வினை என்றழைக்கப்படுகிறது.

குறுக்க கான்னிசரோ வினையில் அதிக வினைதிறன் கொண்ட ஆல்டிஹைடானது ஆக்ஸிஜனேற்றம் அடைகிறது, குறைந்த வினைதிறன் கொண்ட ஆல்டிஹைடு ஒடுக்கமடைகிறது.
3) பென்சாயின் குறுக்கம்
ஒரு அரோமேடிக் ஆல்டிஹைடை நீர்த்த ஆல்கஹாலில் கரைந்த KCN கரைசலுடன் வினைப்படுத்தும்போது, ஹைட்ராக்ஸி கீட்டோன் உருவாகிறது. இவ்வினையானது பென்சாயின் குறுக்கம் என்றழைக்கப்படுகிறது.
எடுத்துக்காட்டு: பென்சால்டிஹைடானது ஆல்கஹாலில் கரைந்த KCN உடன் வினைப்பட்டு பென்சாயினை தருகிறது.
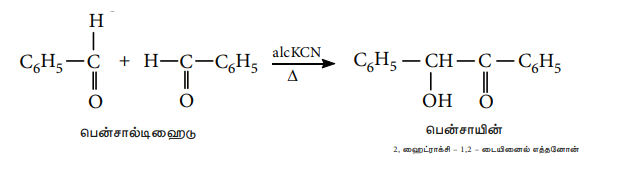
4) பெர்கின் வினை
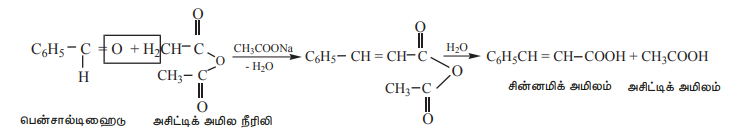
ஒரு அரோமேடிக் ஆல்டிஹைடை, ஒரு அலிஃபாடிக் அமில நீரிலியுடன் சேர்த்து ஒரு அமில நீரிலியுடன் தொடர்புடைய அமிலத்தின் சோடியம் உப்பின் முன்னிலையில் வெப்பப்படுத்தும்போது குறுக்க வினை நிகழ்ந்து ஒரு α,β நிறைவுறா அமிலம் பெறப்படுகிறது. இந்த வினையானது பெர்கின் வினை என அறியப்படுகிறது.
எடுத்துக்காட்டு :
5) நோவெநகல் வினை
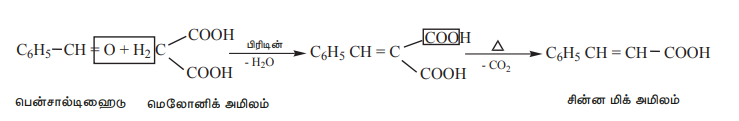
பிரிடின் முன்னிலையில் பென்சால்டிஹைடு ஆனது மலோனிக் அமில மூலக்கூறுடன் குறுக்க வினைக்கு உட்பட்டு சின்னமிக் அமிலத்தை தருகிறது. இவ்வினையில் பிரிடின், கார வினைவேக மாற்றியாக செயல்படுகிறது.
6) அமீன்களுடன் வினை
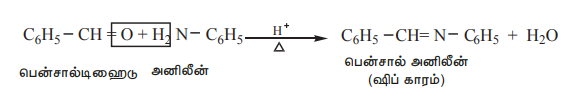
அமிலத்தின் முன்னிலையில், அரோமேடிக் ஆல்டிஹைடுகள், ஓரிணைய அமீன்களுடன் (அலிஃபாடிக் அல்லது அரோமேடிக்) வினைப்பட்டு ஷிஃப் காரத்தை தருகின்றன.
எடுத்துக்காட்டு
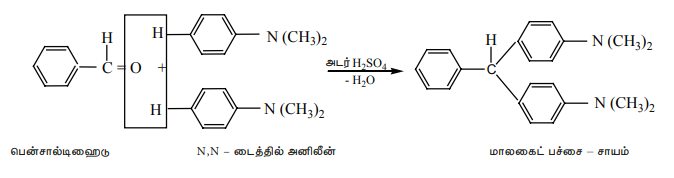
7) மூவிணைய அரோமேடிக் அமீன்களுடன் குறுக்க வினை
வலிமை மிகுந்த அமிலங்கள் முன்னிலையில், பென்சால்டிஹைடானது N, N - டைமெத்தில் அனிலீன் போன்ற அரோமேடிக் அமீன்களுடன் குறுக்க வினைக்கு உட்பட்டு ட்ரைபீனைல் மீத்தேன் சாயத்தை உருவாக்குகிறது.
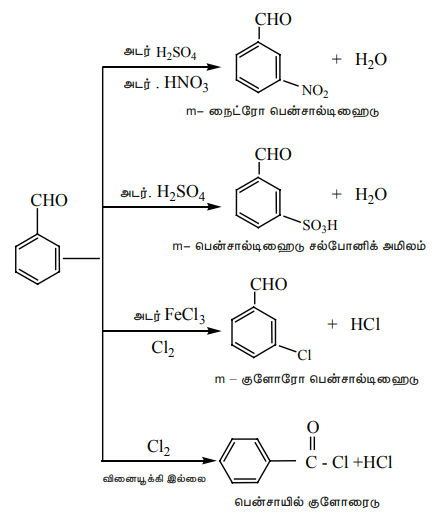
8) பென்சால்டிஹைடின் எலக்ட்ரான் கவர் பதிலீட்டு வினைகள்
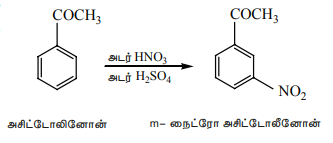
அசிட்டோபீனோனின் எலக்ட்ரான் கவர் பதிலீட்டு வினை
அசிட்டோபீனோன், நைட்ரோ ஏற்ற கலவையுடன் வினைப்பட்டு m - நைட்ரோ அசிட்டோபீனோனை தருகிறது.