12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 12 : கார்பனைல் சேர்மங்கள் மற்றும் கார்பாக்சிலிக் அமிலங்கள்
கார்பாக்சிலிக் அமிலங்களின் அமிலத்தன்மை
கார்பாக்சிலிக் அமிலங்களின் அமிலத்தன்மை
நீரில் கரைக்கப்படும் போது, கார்பாக்சிலிக் அமிலங்கள் அயனியாக்கமடைந்து H+ அயனிகள் மற்றும் கார்பாக்சிலேட் அயனிகளை தருகின்றன. இந்த கார்பாக்சிலேட் அயனிகள் உடனிசைவால் நிலைப்புத்தன்மையை பெறுகின்றன. இதனால் கார்பாக்சிலிக் அமிலங்கள் எளிதாக ஒருபுரோட்டானை இழக்கும் தன்மையினைப் பெறுகின்றன.
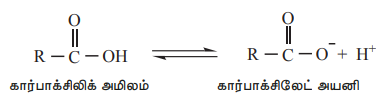
கார்பாக்சிலேட் அயனி கார்பாக்சிலேட் அயனியின் உடனிசைவு அமைப்புகள் கீழே கொடுக்கப்பட்டுள்ளன.
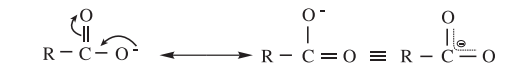
கார்பாக்சிலிக் அமிலங்களின் வலிமையை அவற்றின் பிரிகை மாறிலி (Ka) மதிப்புகள் வாயிலாக குறிப்பிட முடியும்.
R - COOH + H2O ↔ RCOO - + H3O+
Ka = [RCOO-] [H3O+] / [RCOOH]
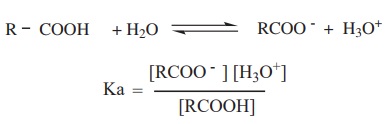
ஒரு அமிலத்தின் பிரிகை மாறிலியானது, அதன் ஒப்பு அமிலத்தன்மையை குறிப்பிடும் அளவாக இருப்பதால், பொதுவாக அமிலத்துவ மாறிலி என்றழைக்கப்படுகிறது. அமிலம் வலிமை மிகுந்ததாக இருப்பின் அதன் Ka மதிப்பு அதிகமாக இருக்கும்.
அமிலத்தின் பிரிகை மாறிலியை அதன் pKa மதிப்பாகவும் குறிப்பிட முடியும்.
pKa = - log Ka
வலிமைமிகு அமிலமானது உயர் Ka மதிப்பையும், தாழ்ந்த pKa மதிப்பையும் கொண்டிருக்கும்.
298 K வெப்பநிலையில் சில கார்பாக்சிலிக் அமிலங்களின் Ka மற்றும் pKa மதிப்புகள்
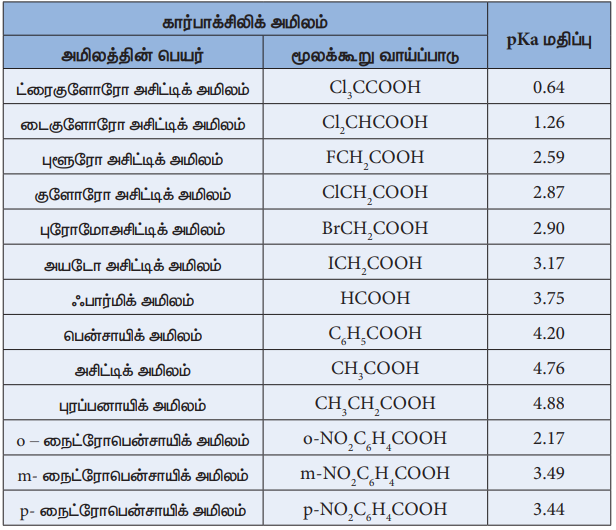
கார்பாக்சிலிக் அமிலங்களின் அமிலத்தன்மை மீதான பதிலிடு தொகுதிகளின் விளைவு.
i) எலக்ட்ரான் உள்தள்ளும் ஆல்கைல் தொகுதி அமிலத்தன்மையை குறைக்கின்றது.
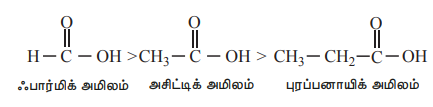
எலக்ட்ரான் உள்தள்ளும் தொகுதிகள் (+I தொகுதிகள்) கார்பாக்சிலேட் அயனியின் மீதுள்ள எதிர்மின்சுமையை அதிகரிப்பதால், அதன் நிலைப்புத் தன்மையை குறைகிறது. இதனால் புரோட்டான் வெளியேற்றம் கடினமாகிறது. எடுத்துக்காட்டாக, ஃபார்மிக் அமிலமானது அசிட்டிக் அமிலத்தை விட அதிக அமிலத்தன்மையை கொண்டுள்ளது.
ii) எலக்ட்ரான் வெளியீர்க்கும் தொகுதிகள் அமிலத்தன்மையை அதிகரிக்கின்றன.
எலக்ட்ரான் வெளியீர்க்கும் தன்மை கொண்ட பதிலிடு தொகுதிகள், கார்பாக்சிலேட் அயனியின் மீதுள்ள எதிர்மின்சுமையை குறைப்பதால், அதன் நிலைப்புத் தன்மையை அதிகரிக்கிறது. இதனால் புரோட்டான் வெளியேற்றம் ஒப்பீட்டளவில் எளிதாக நிகழ்கிறது.
பதிலிகளின் எலக்ட்ரான் கவர்தன்மை அதிகரிக்கும்போது அமிலத்தன்மையும் அதிகரிக்கிறது. எடுத்துக்காட்டாக, பல்வேறு ஹேலோ அசிட்டிக் அமிலங்களின் அமிலத்தன்மை பின்வரும் வரிசையில் அமைகிறது.
F – CH2 – COOH > Cl-CH2 - COOH>Br-CH2 - COOH > I – CH2 - COOH
α - கார்பனில் இணைந்துள்ள எலக்ட்ரான் வெளியீர்க்கும் தொகுதிகளின் எண்ணிக்கை அதிகரிக்கும்போது அமிலத்தன்மை அதிகரிக்கிறது. எடுத்துக்காட்டாக
Cl3C- COOH > Cl2CH - COOH > ClCH2COOH > CH3COOH
கார்பாக்சிலிக் அமிலத்தின் அமிலத்தன்மை மீதான பல்வேறு எலக்ட்ரான் வெளியீர்க்கும் தொகுதிகளின் விளைவுகள் பின்வரும் வரிசையில் அமைகிறது.,
- NO2 > - CN > - F > - Cl > - Br > - I > Ph
பல்வேறு கரிம சேர்மங்களின் ஒப்பு அமிலத்தன்மை பின்வருமாறு
RCOOH > ArOH > H2O > ROH > RC ≡ CH