வளம், இயற் பண்புகள், வேதிப் பண்புகள், பயன்கள் - பதினெட்டாவது தொகுதி தனிமங்கள் (மந்த வாயுக்கள்) | 12th Chemistry : UNIT 3 : p-Block Elements-II
12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 3 : P-தொகுதி தனிமங்கள் -II
பதினெட்டாவது தொகுதி தனிமங்கள் (மந்த வாயுக்கள்)
பதினெட்டாவது தொகுதி தனிமங்கள் (மந்த வாயுக்கள்)
கிடைக்கபெறுதல்
அனைத்து மந்த வாயுக்களும் வளிமண்டலத்தில் காணப்படுகின்றன.
இயற் பண்புகள்
மந்தவாயுத் தொகுதி தனிமங்களில் மேலிலிருந்து கீழாக ஹீலியத்திலிருந்து, ரேடானனை நோக்கி வரும் போது அவைகளின் அயனி ஆரங்கள் மற்றும் கொதிநிலைகள் அதிகரிக்கின்றன. முதல்அயனியாக்கும் ஆற்றல் ஹீலியத்திலிருந்து ரேடானை நோக்கி வரும் குறைகிறது. மந்த வாயுக்கள் அவை இடம்பெற்றுள்ள வரிசையில் உள்ள மற்ற அனைத்து தனிமங்களைக் காட்டிலும் அதிகமான அயனியாக்கும் ஆற்றலை பெற்றுள்ளன. ஏனெனில், இவைகள் தங்கள் வெளிக்கூட்டில் முழுவதும் நிரப்பப்பட்ட ஆர்பிட்டால்களை பெற்றுள்ளன. இவைகள் மிகவும் நிலைப்புத் தன்மையுடையவை. எலக்ட்ரானை ஏற்கும் அல்லது இழக்கும் தன்மையினை மிகக் குறைந்தளவே பெற்றுள்ளன. பதினெட்டாம் தொகுதி தனிமங்களின் இயற்பண்புகள் பின்வரும் அட்டவணையில் தரப்பட்டுள்ளன.
அட்டவணை 3.10 பதினெட்டாம் தொகுதி தனிமங்களின் இயற்பண்புகள்
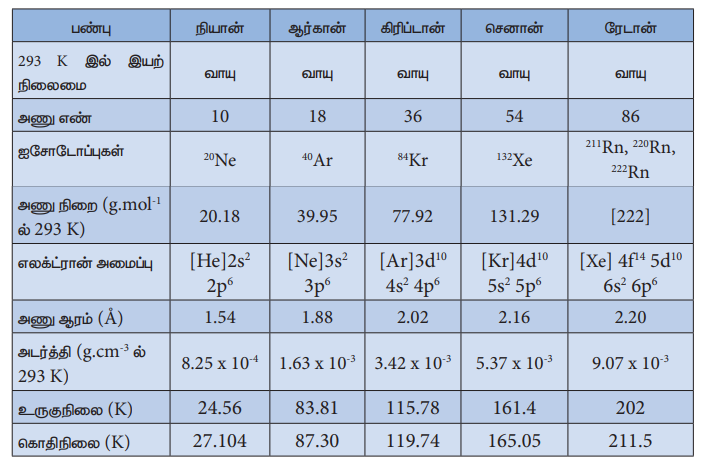
மந்த வாயுக்களின் பண்புகள்
இயற்பண்புகள்
மந்தவாயுக்கள் அனைத்தும் ஓர் அணுகளைக் கொண்டவை. நிறம், மணம் மற்றும் சுவை அற்றவை. இவைகள் எளிதில் தீப்பற்றி எரியாத் தன்மையுடையவை. இவைகள் அதிகளவு வினைத்திறன் அற்றவை. உலோகத் தன்மையற்றவை
வேதிப் பண்புகள்
செனான் மற்றும் கிரிப்டான் ஆகியன மட்டும் குறைந்த அளவு வேதி வினைத்திறனை பெற்றுள்ளன. செனானை புளூரினுடன் கீழ்கண்டுள்ளவாறு வெவ்வேறு நிபந்தனைகளில் வினைப்படுத்தும் போது செனான் புளூரைடுகள் உருவாகின்றன.
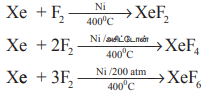
XeF6 யை ஒரு மூடப்பட்ட குவார்ட்ஸ் கலனில் 50°C வெப்பநிலையில் வெப்பப்படுத்துபோதும். XeOF4 உருவாகிறது.
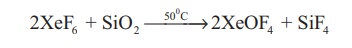
2XeF6 + SiO2 →50 0 C →2XeOF4 + SiF4
வினையைத் தொடர்ந்து நிகழ்த்தும் போது பின்வரும் வினைகள் நடைபெறுகின்றன.
2XeOF4+ SiO2 → 2XeO2F2 + SiF4
2XeO2F2 + SiO2 → 2XeO2 + SiF4
நீராவியால் நீராற்பகுப்பின் போது XeF6 ஆனது XeO3 யைத் தருகிறது.
XeF6+ 3H2O → XeO2 + 6HF
XeF6 யை 2.5M NaOH யுடன் வினைபடுத்தும்போது சோடியம் பெர்சினேட் உருவாகிறது.
2XeF6 + 16NaOH → Na4XeO6 + Xe + O2 + 12NaF + 8HO2
சோடியம் பெர்சினேட் ஒரு வலிமையான ஆக்சிஜனேற்றும் வினைப்பொருளாகும். எடுத்துக்காட்டாக இது மாங்கனீஸ் (II) அயனியை வினைவேக மாற்றி ஏதும் இல்லாத நிலையில் கூட பெர்மாங்கனேட் அயனியாக ஆக்சிஜனேற்றமடையச் செய்கிறது.
5XeO64-+ + 2Mn2+ + 14H+ → 2MnO4- + 5XeO3 + 7H2O
செனான் PtF6 யுடன் வினைபட்டு ஆரஞ்சு மஞ்சள் நிற திண்மம் (XePtF6) தருகிறது. இது CC14 யில் கரைவது இல்லை .
செனான்டைபுளூரோரைடானது XeF2-2SbF5 மற்றும் XeF2-2TaF5 ஆகிய சேர்க்கை சேர்மங்களை தருகிறது. செனான் ஹெக்சாபுளூரைடானது போரன் மற்றும் கார உலோகங்களுடன் XeF6.BF3’ XeF6MF சேர்மங்களைத் தருகிறது. .M- கார உலோகங்கள்.
செனான் டைகுளோரைடு இருப்பதற்கான சில ஆதாரங்கள் உள்ளன.
கிரிப்டான் மற்றும் புளூரின் ஆகியனவற்றின் வழியே 183 மின்பாய்ச்சலை செலுத்தும் போது கிரிப்டான் டைபுளூரைடு உருவாகிறது. கிரிப்டான் வாயுவை SbF5 சேர்த்து கதிர்வீச்சலுக்கு உட்படுத்தி வினைபடுத்தும் போது KrF22SbF3. உருவாகிறது.
அட்டவணை 3.11 செனான் சேர்மங்களின் வடிவமைப்புகள்
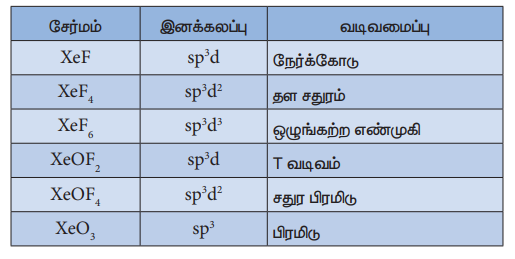
மந்த வாயுக்களின் பயன்கள்
மந்தவாயுக்களின் முக்கிய பயன்பாட்டிற்க்கு அவைகளின் வேதியியல் மந்தத்தன்மையே காரணமாகும்.
ஹீலியம்
1. ஹீலியம் மற்றும் ஆக்சிஜன் கலவையானது காற்றும் மற்றும் ஆக்சிஜன் கலவைக்கு மாற்றாக நீர்மூழ்குபவர்களால் பயன்படுத்தபடுகிறது. இது வளைவு என்று அழைக்கப்படும் ஆபத்தான வலி ஏற்படுத்தும் நிகழ்வினை தடுக்கிறது.
2. மின்வில் முறையில் உலோகங்களை ஒட்டும் செயல்முறையில் மந்த வினைபுரியா சூழலை ஏற்படுத்த ஹீலியம் பயன்படுகிறது.
3. ஹீலியமானது குறைவான கொதிநிலையைக் கொண்டிருப்பதால் கிரையோஜெனிக் நுட்பங்களில் பயன்படுகிறது.
4. காற்றைவிட லேசானது என்பதால் காற்றில் மிதக்கும் பலூன்களிலுள் நிரப்பப் பயன்படுகிறது.
நியான்
குறைந்த அழுத்தத்தில், நியான் வாயுவின் வழியே மின்சாரத்தை செலுத்துவதால் பிரகாசமான சிகப்பு நிற ஒளிர்தல் ஏற்படுகிறது. இப்பண்பினால் நியான் விளம்பர பலகைகளில் பயன்படுகிறது.
ஆர்கான்
சூடானமின்னிழைகளில் ஆக்சிஜனேற்றம் ஏற்படுவதை ஆர்கான் தடுக்கிறது. இதனால் பல்புகளில் காணப்படும் மின்னிழைகளின் ஆயுள் நீட்டிக்கப்படுகிறது.
கிரிப்டான்
ஒளிரும் பல்புகள், ஒளிவீச்சு பல்புகள் ஆகியனவற்றில் பயன்படுகிறது.
கிரிப்டானை நிரப்பப்பட்ட விளக்குகள் ஒளிரும் ஒளியானது அடர்ந்த பனிபுகையினையும் ஊடுருவும் தன்மையுடையதால் இத்தகைய விளக்குகள் விமான நிலையங்களில் அணுகும் விளக்குகளாக பயன்படுகின்றன.
செனான்
ஒளிரும் பல்புகள், ஒளிவீச்சு பல்புகள் மற்றும் லேசர்கள் ஆகியனவற்றில் பயன்படுகிறது. மின்னிறக்க குழாய்களில் செனான் உடனடியாக செறிவு மிக்க ஒளியை உமிழும் தன்மையைக் கொண்டது. இப்பண்பின் காரணமாக புகைப்பட நிபுணர்கள் பயன்படுத்தும் அதிவேக மின்பாய்ச்சல் விளக்குகளில் பயன்படுகிறது.
ரேடான்
ரேடான் கதிரியக்கத்தன்மையுடையது. மேலும் காமா கதிர்வீச்சிற்கு ஒரு மூலமாக பயன்படுகிறது. ரேடான் வாயுவானது சிறிய குப்பிகளில் அடைக்கப்பட்டு புற்றுநோயாளிகளின் உடலினுள் வைக்கப்படும் போது அவை புற்று நோய் செல்களை அழிக்கின்றன.