12 ஆம் வகுப்பு வேதியியல் : அத்தியாயம் 3 : P-தொகுதி தனிமங்கள் -II
பாஸ்பரஸின் பண்புகள் மற்றும் பயன்கள்
பாஸ்பரஸின் பண்புகள்
பாஸ்பரஸ் அதிக வினைத்திறன் கொண்டது. இது பின்வரும் முக்கிய வேதிப்பண்புகளைப் பெற்றுள்ளது.
ஆக்ஸிஜனுடன் வினை: மஞ்சள் நிற பாஸ்பரஸ், காற்றில் தானாக தீப்பற்றி எரிந்து பாஸ்பரஸ் பென்டாக்சைடு வெண்புகையைத் தருகிறது. சிவப்பு பாஸ்பரஸும் வெப்பப்படுத்தும் போது ஆக்ஸிஜனுடன் வினைப்பட்டு பாஸ்பரஸ் ட்ரை ஆக்ஸைடு அல்லது பாஸ்பரஸ் பென்டாக்சைடைத் தருகிறது.
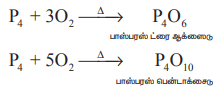
குளோரினுடன் வினை: பாஸ்பரஸ், குளோரினுடன் வினைப்பட்டு ட்ரை மற்றும் பென்டா குளோரைடுகளை தருகிறது.அறை வெப்பநிலையில் மஞ்சள் பாஸ்பரஸ் தீவிரமாக வினைபுரிகிறது, ஆனால் சிவப்பு பாஸ்பரஸ் வெப்பப்படுத்தும்போது மட்டும் வினைபுரிகிறது.
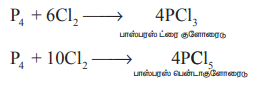
P4 + 6C12 → 4PC13
பாஸ்பரஸ் ட்ரை குளோரைடு
P4 + 10C12 → 4PC13
பாஸ்பரஸ் பென்டாகுளோரைடு
காரங்களுடன் வினை : மஞ்சள் பாஸ்பரஸை, மந்த வாயுச்சூழலில் காரங்களுடன் சேர்த்து கொதிக்கவைக்கும்போது பாஸ்பீன் வாயுவை வெளியேற்றுகிறது. இதில் பாஸ்பரஸ் ஒடுக்கும் காரணியாக செயல்படுகிறது.
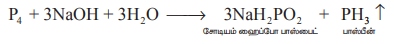
P4 + 3NaOH + 3H2O → 3NaH2PO2 + PH3 ↑
சோடியம் ஹைப்போ பாஸ்பைட் பாஸ்பீன்
நைட்ரிக் அமிலத்துடன் வினை : பாஸ்பரஸை அடர் நைட்ரிக் அமிலத்துடன் வினைப்படுத்தும்போது, பாஸ்பாரிக் அமிலமாக ஆக்ஸிஜனேற்றமடைகிறது. இவ்வினையில் படிக அயோடின் வினைவேகமாற்றியாக செயல்படுகின்றன.

P4 + 20HNO3 → 4H3PO4 + 20NO2 + 4H2O
ஆர்த்தோ பாஸ்பாரிக் அமிலம்
உலோகங்களுடன் வினை: Ca மற்றும் Mg போன்ற உலோகங்களுடன் பாஸ்பரஸ் வினைப்பட்டு பாஸ்பைடுகளைத் தருகிறது. சோடியம் மற்றும் பொட்டாசியம் போன்ற உலோகங்கள் வீரியமுடன் வினைபுரிகின்றன.
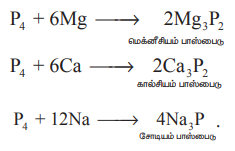
P4 + 6Mg → 2Mg3P2
மெக்னீசியம் பாஸ்பைடு
P4 + 6Ca → 2Ca3P2
கால்சியம் பாஸ்பைடு
P4 + 12Na → 4Na3P .
சோடியம் பாஸ்பைடு
பாஸ்பரஸின் பயன்கள்:
1. தீப்பெட்டிகளில் சிவப்பு பாஸ்பரஸ் பயன்படுகிறது.
2. இது, பாஸ்பரஸ் வெண்கலம் போன்ற உலோகக் கலவைகள் தயாரிப்பிலும் பயன்படுத்தப்படுகிறது.